
最近のトピックス 2012/12/20
歯根の形成に関わる疾患の原因解明と治療法の模索
岩手医科大学 統合基礎講座
解剖学講座 発生生物・再生医学分野
教授 原田英光,大学院生 坂野深香
電話 019−651−5110 内線5881
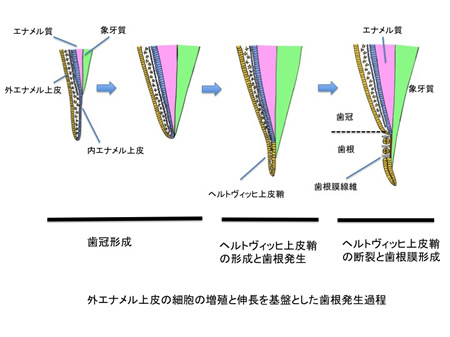
歯は歯冠と歯根の2つのパートからできていますが,歯冠のでき方を調べる研究に比べ,歯根がどのようにしてできるのかということを追求した研究はあまり多くありません。しかし,先天的に歯根が無いことや極端に短い症例を見かけることがあります。いろいろな原因が考えられるのですが,そのひとつとして歯根形成を誘導するヘルトヴィッヒ上皮鞘の細胞の動きが重要であることが最近の研究からわかってきました。教科書的には,このヘルトヴィッヒ上皮鞘は内外のエナメル上皮が合わさって伸びていくことで形成されると考えられていましたが,我々の研究から主に外エナメル上皮の細胞が増殖して伸びていくことが重要であるとわかりました。内エナメル上皮はエナメル芽細胞に分化してエナメル質の形成に直接関与する細胞として知られています。内エナメル上皮の細胞は増殖して歯冠の外形を形作ると,これらの細胞はあまり活発に動かなると同時にエナメル基質を大量に分泌します。一方,外エナメル上皮の細胞は増殖と移動を繰り返して,ヘルトヴィッヒ上皮鞘の形成に関わるようになります(図1)。ヘルトヴィッヒ上皮鞘の形成過程を示すビデオはhttp://www.youtube.com/watch?v=tDtAY3-63cY&feature=youtu.beをご覧下さい。
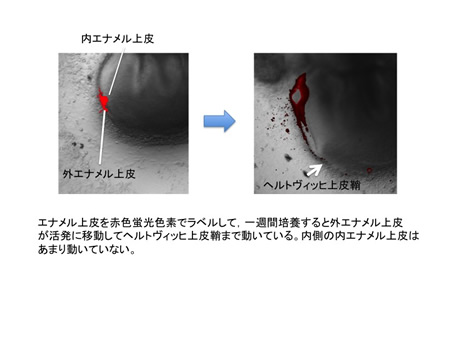
今回の研究では,私たちは生きた状態の生の標本を作製して,特殊な顕微鏡で細胞の分裂や動きを直接見ることでこれらの現象を明らかにしました。また,蛍光色素を使った観察方法では外エナメル上皮細胞が内エナメル上皮の細胞よりもより活発に歯根方向へ動いている様子も見ることができました(図2)。この研究成果は,歯根形成のメカニズムに新説を投げかけると共に,歯根の形成に関わる疾患の原因解明や治療法の開発に生かせると考えています。前回の号で,HGFの話をしましたが,これもまた外エナメル上皮の細胞の増殖と移動を推進させる因子のひとつであります。これらの研究を進めることで,歯根未完成歯の歯根の成長を誘導する治療法開発につなげたいと思っています。
§この内容はJ. Periodont. Res., Article first published online : 14 SEP (2012)に掲載されました。
最近のトピックス 2012/5/17
肝細胞増殖因子による新しい歯周組織再生
歯は口の中に出ている歯冠とあごの骨に埋まっている歯根に分けられます。歯根は表面をセメント質と言う硬い組織で被われていますが、ただ歯根の表面にセメント質があるというだけでなく、セメント質は歯根膜を仲立ちにして骨とつながれており、それぞれの組織が連携して機能を果たします。そして、これらをひとまとめにして歯周組織と言います。歯科矯正の治療中に歯根が吸収されて短くなってしまったり、外傷などによって歯根の形成に障害が及んだりする場合があり、これらを治療するためには、歯根の成長を誘導する技術開発が必要ですが、このような場合でも、ただ歯根だけを作れば良いというものではなく、歯周組織全体の形成促進をはかる必要があります。しかし、歯根の形成メカニズムはまだよく分かっていないことも多く、私たちの研究室では、歯根の形成を促進する因子について研究を進めています。
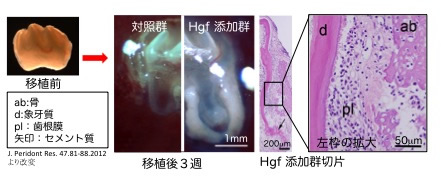
今回私たちは肝細胞の増殖を促進する因子として発見され、最近様々な組織の再生医療に用いられている肝細胞増殖因子(HGF)に注目しました。マウスのまだ歯根が形成されていない歯の原基(歯胚)の芯にある組織(歯髄)にHGFをしみ込ませた小さなビーズを埋め込んで、腎被膜下移植法(マウス腎臓の被膜の下に移植物を埋め込んで育てる方法)を使って歯胚を3週間育てました。するとHGFを加えた歯胚はHGFを作用させていない(対照群)歯胚に比べて歯根の成長が進み、長い歯根が形成されました。さらには移植を始める前にはなかった、歯根膜や骨などの歯周組織も作られていることが分かりました(図)。
HGFは、歯根の伸長や歯周組織の再生が併せて促進できることから、現在、臨床研究されているサイトカイン(FGF-2)療法に代わる、あるいはそれに匹敵する新たな因子として、歯周組織の再生医療への応用が期待できると考えています。
※ この内容はJ. Periodont. Res., 47:81-88. (2012)に掲載されました。
岩手医科大学 統合基礎講座
解剖学講座 発生生物・再生医学分野
教授 原田 英光、講師 藤原 尚樹
電話 019-651-5111(内線5881
最近のトピックス 2012/4/5
歯胚細胞へのグルコース取り込み調節が歯の発育に及ぼす影響
グルコースは生体の主要なエネルギー源であり、細胞外のグルコースは細胞膜上に発現されるグルコース輸送体(GLUT)によって細胞質内へ取り込まれ、グリコーゲンとして貯蔵される。歯の発育においても、このようなグルコース代謝が重要であることは容易に想像されるものの、具体的な役割については解明されていなかった。本研究では、歯胚発育過程におけるグルコースの動態とGLUTの発現様式を同定し、さらに、歯胚細胞へのグルコースの取り込み量を調節することにより、発育歯胚の大きさが変化することを世界で初めて証明した。
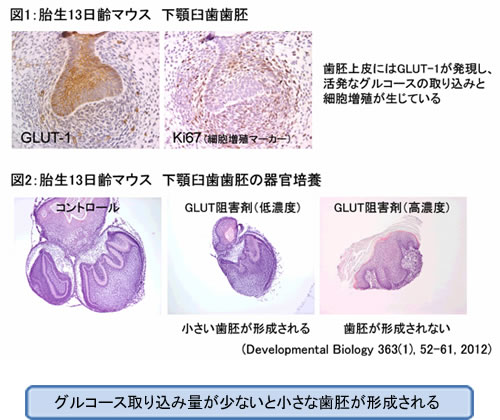
マウス歯胚の発育初期では、細胞増殖の盛んな歯胚上皮にグルコース結合能の高いI型GLUT(GLUT-1)が発現しており(図1)、同時期の歯胚にGLUT-1阻害剤を作用させて培養を行うと、歯胚形成が完全に停止した。さらに、阻害剤の濃度を調節して少量のグルコースが取り込まれる環境にすると、小さな歯胚が形成された(図2)。従って、GLUT-1を介した歯胚細胞へのグルコースの取り込みは、歯胚の初期発育に必須であり、歯胚の大きさに影響を与えることが明らかとなった。
本研究は、歯胚におけるグルコース取り込みの分子メカニズム、ならびに栄養状態が歯の発育に及ぼす影響についての一端を培養系で証明した初めての研究成果であり、将来的に歯の発育におけるグルコース代謝の詳細なプロセスが明確になれば、糖代謝異常による歯の形成不全などの疾患の原因究明や治療法の開発につながることが期待される。
この研究は岩手医科大学解剖学講座発生生物・再生医学分野の原田英光教授との共同研究で、2012年のDevelopmental Biologyに掲載されました。
新潟大学 大学院医歯学総合研究科
顎顔面再建学講座 硬組織形態学分野
教授 大島 勇人
准教授 依田 浩子
電話:025-227-2812, 2813
最近のトピックス 2012/3/1
iPS細胞からエナメル質をつくるエナメル芽細胞の誘導に成功
歯はエナメル質と象牙質よりつくられており、その中でもエナメル質は体の中で最も硬い組織です。象牙質をつくる象牙芽細胞は歯を形成した後も歯髄の中に存在し続けますが、エナメル芽細胞は、歯が萌出する(生える)と、体の中に存在しなくなります。
このためエナメル芽細胞がどのように分化し機能を維持しているのか明らかでなく、そのメカニズム解明や、これらの細胞を歯の再生に応用する為には、マウスの胎仔を利用しなければなりませんでした。
歯は口腔内の上皮とその下に存在する間葉系細胞との相互作用により形成されます。この上皮細胞との相互作用により、様々な細胞がどのような運命をたどるかを解明する過程で、人工多能性幹細胞(iPS細胞)から、エナメル質をつくるエナメル芽細胞の誘導に成功しました。
これは東北大学病院の新垣真紀子医員、歯学研究科の福本敏教授らと、米国国立衛生研究所(山田吉彦主任他)、岩手医科大学(原田英光教授他)、東京理科大学(齋藤正寛准教授)との共同研究による成果です。
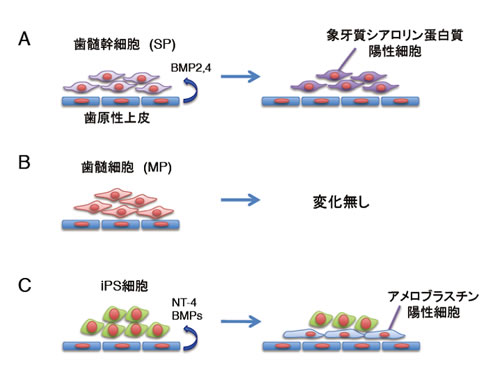
今回、研究グループは、ラット由来の歯原性上皮細胞とマウス由来iPS細胞を共培養することで、iPS細胞がエナメル基質であるアメロブラスチン、エナメリン(エナメル芽細胞マーカー)を発現することを確認しました。
また、この分化過程において分化誘導に用いた細胞から分泌されるNT-4(神経栄養因子の1つ), BMPやアメロブラスチンが重要な役割を演じていることを明らかにしました。具体的には、iPS細胞のような万能細胞は、歯原性上皮との相互作用により、相互作用させたもとの細胞(アメロブラスチン陽性の歯原性上皮)に分化誘導されます。歯髄幹細胞のように、多分化能を有するが、個体発生が不可能な細胞は、上皮との相互作用で象牙芽細胞(象牙質シアロリン蛋白陽性細胞)に分化します。
しかしながら、既に最終分化した細胞は、上皮細胞との相互作用により、エナメル芽細胞にも象牙芽細胞にも分化しません。この成果は、今まで困難であったエナメル芽細胞の役割を明らかにすること、さらには歯の再生の為の細胞ソースとして応用可能な新しい技術です。
本研究成果は、米国の科学雑誌「The Journal of Biological Chemistry」電子版に掲載されました。
*本研究の成果は、内閣府の最先端・次世代研究開発支援プログラム「かたちに関わる疾患解明を目指した歯の形態形成メカニズムの理解とその制御法の開発」(研究代表者:福本敏 東北大学大学院歯学研究科教授)によるものです。
最近のトピックス 2011/12/15
iPS細胞から歯の象牙芽細胞への分化誘導技術の開発について
歯の表面はエナメル質でその内側は象牙質で作られており,エナメル質はエナメル芽細胞によって象牙質は象牙芽細胞で作られる。本発明は iPS 細胞から象牙芽細胞の特性をもった細胞に分化誘導する技術を世界で始めて開発した。
象牙芽細胞の祖先は外胚葉に由来する神経堤細胞であり,この細胞は歯胚の上皮細胞(エナメル質を作るもとの細胞)とふれあうことで歯胚の間葉細胞(歯を作る結合組織側の細胞)になり,その後象牙芽細胞となることが知られている。
我々の発明した方法はまずiPS細胞を神経堤細胞に分化させ,その後、この神経堤細胞を歯胚上皮細胞と組み合わせて共培養することや、歯胚上皮細胞の培養上清を培地に加えたりすることでこの細胞が象牙芽細胞を含む歯原性間葉へと分化すること、また誘導した神経堤細胞の中からより象牙芽細胞へ分化する能力が強い細胞を見いだして,効率的にiPS細胞から象牙芽細胞へ分化誘導する方法を確立した。
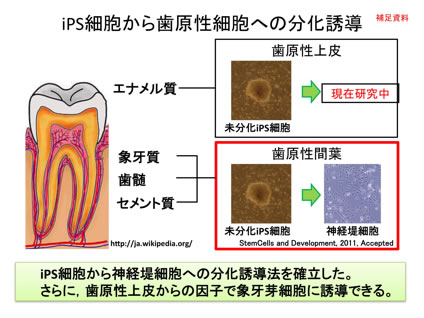
象牙芽細胞が生まれる過程で上皮細胞との非常に複雑な分化調節機構が働いているため,iPS細胞を象牙芽細胞へと分化させることは非常に困難であった。
本発明は、段階的にiPS細胞を分化させることによってこの問題を克服し、象牙芽細胞を効率よく獲得することを可能にした。
将来的には,歯の形成に関わる上皮細胞もiPS細胞から作ることが可能になれば,iPS細胞を使って歯を再生させることも可能になるだろう。また,遺伝的に歯ができない患者様の研究モデルも作ることができ,今後の治療法開発にも生かせることができる。
この研究は東北大学歯学研究科小児発達歯科学分野福本敏教授との共同研究で,Stem Cells & Developmentのon line版に発表されました。
岩手医科大学 統合基礎講座
解剖学講座 発生生物・再生医学分野
教授 原田 英光
研究員 大津 圭史
電話:019-651-5111(内線5880、5881)